la maladie veineuse chronique : Clinique et score
France | 27 mars 2018
Vous découvrirez ci-dessous le Chapitre 3 Clinique et score de l’ouvrage La maladie veineuse chronique.
Cet ouvrage est épuisé mais son contenu est repris dans le Traité de médecine vasculaire - Offre Premium S’ouvre dans une nouvelle fenêtre, qui synthétise en un volume l'ensemble des connaissances en médecine cardiovasculaire, tous domaines confondus, en un livre papier et un accès exclusif à la version complète en eBook.
Le traité de référence en médecine vasculaire
1. Bases fondamentales. 2. Explorations vasculaires. 3. Maladies artérielles. 4. Maladies veineuses. 5. Lymphologie. 6. Malformations et tumeurs vasculaires. 7. Microcirculation. 8. Ulcères de cause vasculaire. 9. Situations particulières. 10. Thérapeutique.
Traité de médecine vasculaire - Offre Premium Le livre papier + votre accès à l'ebook du traité complet
SFMV, CEMV, CFPV ISBN 9782294768095 2021

Traité de médecine vasculaire - Offre Premium
Clinique et score
Plan du chapitre
Motif de consultation
Interrogatoire initial
Examen clinique
Scores cliniques
L’examen clinique dans notre pratique quotidienne est orienté par le motif de consultation [1].
Motif de consultation
Tout d’abord, le médecin s’attache à préciser la demande du patient. Le plus souvent cette dernière est liée à un symptôme fonctionnel, un désir esthétique ou une varice, plus rarement un œdème, un trouble trophique ou un ulcère. Parfois le motif est vague « j’ai une mauvaise circulation » ; il convient alors de faire préciser par la question : « Une mauvaise circulation, ça veut dire quoi pour vous ? »
Puis, il est nécessaire d’insister pour connaître un éventuel motif secondaire, parfois plus difficile à exprimer, comme le souhait d’obtenir un second avis thérapeutique, un dépistage, en posant la question : « Que désirez-vous, que souhaitez-vous réellement ? »
Ce préalable indispensable va permettre d’orienter au mieux la suite de l’examen, de répondre à la demande et d’augmenter la probabilité de satisfaire l’attente du patient.
Interrogatoire initial
Cet interrogatoire d’ordre général comprend nécessairement :
nom, prénom, date de naissance, adresse, téléphone, profession, facteurs de risque athéromateux, traitements, allergie, interventions chirurgicales, fractures, plâtres, antécédents de maladie thrombo-embolique y compris dans la famille, maladies particulières ;
évaluation des facteurs de risque de l’insuffisance veineuse superficielle [2–5] à savoir : hérédité, âge, sexe, nombre de grossesses, poids et taille, sédentarité/activité physique.
L’anamnèse en rapport avec le motif de consultation est détaillée.
Examen clinique
L’examen proprement dit commence avec le patient debout sur un escabeau de phlébologie, membres inférieurs nus jusqu’à l’aine, sans pansement ou contention. L’examen se fait de bas en haut, des orteils à la taille, un membre après l’autre en relâchement musculaire et en demandant au patient de tourner.
Puis l’examen se poursuit avec le patient allongé sur une table d’examen.
Debout ou couché, l’éclairage des membres doit être de bonne qualité afin de bien visualiser les vaisseaux et de limiter les ombres portées.
Afin de refléter la réalité, nous présentons la description de l’examen clinique en fonction du motif de consultation tout en suivant le plan de la classification CEAP, rubrique Clinique [6, 7].
C0, A : prévention
Le plus souvent, il s’agit d’un patient anxieux qui a besoin d’être rassuré. L’interrogatoire ne retrouve ni douleur ni œdème en fin de journée. Les facteurs de risque d’insuffisance veineuse superficielle (IVS) sont recherchés.
Les premières varices visibles sont souvent présentes au niveau du genou. Ainsi, pour retrouver les premiers signes physiques de la maladie, l’observation est insistante en haut de jambe et en bas de cuisse, sans oublier la fosse poplitée.
Ici, l’inspection des membres et la palpation–percussion des quatre axes – grandes et petites saphènes – sont rigoureusement normales.
Si une échographie est jugée nécessaire, les mesures des diamètres des quatre axes saphènes sont réalisées de façon standardisée.
À l’issue de la consultation, le patient est rassuré et reçoit des conseils afin notamment de corriger au mieux les facteurs de risque. L’intérêt d’un suivi est évalué.
C0,S : douleurs des membres inférieurs (lourdeurs de jambes)
Les lourdeurs de jambes représentent un motif fréquent de consultation et sont classées dans les douleurs.
D’après une étude française réalisée sur plus de 3 500 patients âgés en moyenne de 46 ans, ceux qui poussent pour la première fois la porte du cabinet du médecin généraliste au motif d’une insuffisance veineuse souffrent d’abord de lourdeurs de jambes dans 70 % des cas [8].
L’interrogatoire revêt une importance considérable pour préciser la douleur [9, 10].
Le score suivant permet de caractériser la douleur de l’insuffisance veineuse chronique :
lourdeur ou pesanteur ou sensation de gonflement (1 point) ;
phlébalgie ou prurit ou impatiences (1 point) ;
aggravée par la chaleur, diminuée par le froid (1 point) ;
non aggravée par la marche (1 point).
Si le score est supérieur à 2, le rapport de cette douleur avec une affection veineuse chronique est hautement probable ; s’il est inférieur à 2, l’imputabilité est improbable [11].
Les critères douleur diffuse de membre et douleur augmentant en cours de journée ne sont pas assez spécifiques ; crampe, élancement, fourmillement, déchirure sont plutôt en faveur d’autres diagnostics [12–14] :
Éléments en faveur du syndrome des jambes sans repos (SJSR)
Nécessité de bouger les membres + dysesthésie ou paresthésie.
Aggravation au repos, amélioration par la marche ou le mouvement.
Mouvements involontaires diminuant l’inconfort.
Aggravation le soir ou la nuit (insomnie d’endormissement).
Cette affection touche 8 % de la population avec des antécédents familiaux dans 40 à 90 % des cas.
Éléments en faveur d’une douleur rhumatologique
Topographie plus localisée de la douleur.
Douleur positionnelle ou liée à un mouvement.
Douleur mécanique.
Douleur inflammatoire en seconde partie de nuit.
Éléments en faveur d’une douleur neurologique
Dysesthésie, fourmillements, décharge électrique.
Douleur sur un trajet nerveux ou concernant un territoire neurologique, en chaussettes.
Trouble objectif de la sensibilité (diapason, filament Nylon).
Abolition d’un réflexe tendineux (achilléen, rotulien).
Les douleurs avec claudication intermittente ont une autre origine :
canal lombaire étroit : soulagée par la position penchée en avant ou assise ;
artériopathie : sujet tabagique, pouls pédieux, indice de pression systolique (IPS) < 0,9 ;
thrombose veineuse profonde : grosse jambe cyanosée.
« Syndrome de la couette »
Ce syndrome est lié à une intolérance à certains couchages trop chauds (couette ou édredon) laissant difficilement passer la vapeur d’eau. Le patient est obligé de mettre ses jambes hors de la couette au cours de la nuit.
Au terme de l’examen clinique et paraclinique, l’origine de la douleur est le plus souvent parfaitement caractérisée. Si un doute subsiste, l’avis d’un rhumatologue ou d’un neurologue peut être utile, ou le port d’une compression peut être proposé pour affiner un diagnostic.
C1 : télangiectasies et demande esthétique
Cette demande est exprimée clairement ou sous-entendue chez un tiers des patients consultant en phlébologie. Il n’en demeure pas moins que les télangiectasies et veinules réticulaires (fig. 3.1) font partie des affections veineuses chroniques et à ce titre ce motif de consultation permet d’en faire le bilan. L’examen élimine les éléments des formes plus sévères de la maladie [15–22].
Les télangiectasies sont des dilatations intradermiques du plexus veineux sous-papillaire. Visibles à l’œil nu, elles sont inférieures à 1 mm. Leur forme est fonction des données locales de circulation.
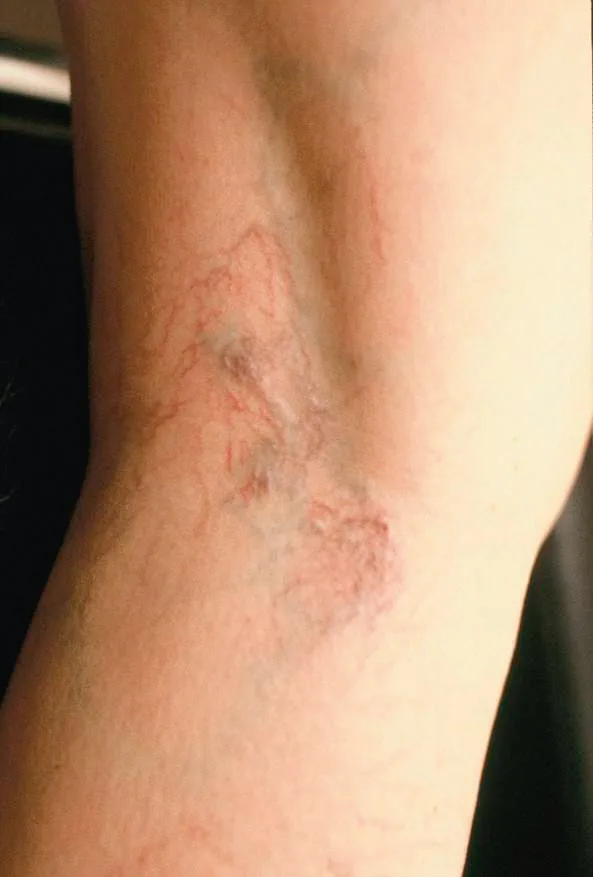
Fig. 3.1 S’ouvre dans une nouvelle fenêtre C1 : veinules et télangiectasies de la fosse poplitée.
Classiquement, on distingue les formes sinueuses, arborisées, en éventail, en araignée, en étoile ou ponctiformes. Leur coloration dépend de la teinte de la peau, de leur diamètre, de leur profondeur dans le derme et du degré d’oxygénation de leur sang. Les télangiectasies rouges sont fines et superficielles. Elles sont isolées ou alimentées par une veine « nourricière » parfois visible sous bon éclairage ou par épiscopie en plaquant directement une source de lumière froide sur la peau en regard. Les télangiectasies s’effacent à la vitropression.
Leur localisation est plus fréquente en face latérale de cuisse, en face médiale de genou, au niveau de la fosse poplitée et de la cheville (fig. 3.2).
Elles apparaissent progressivement au cours de la vie, parfois à l’occasion d’une grossesse, d’une prise de poids importante ou d’une exposition aux ultraviolets.
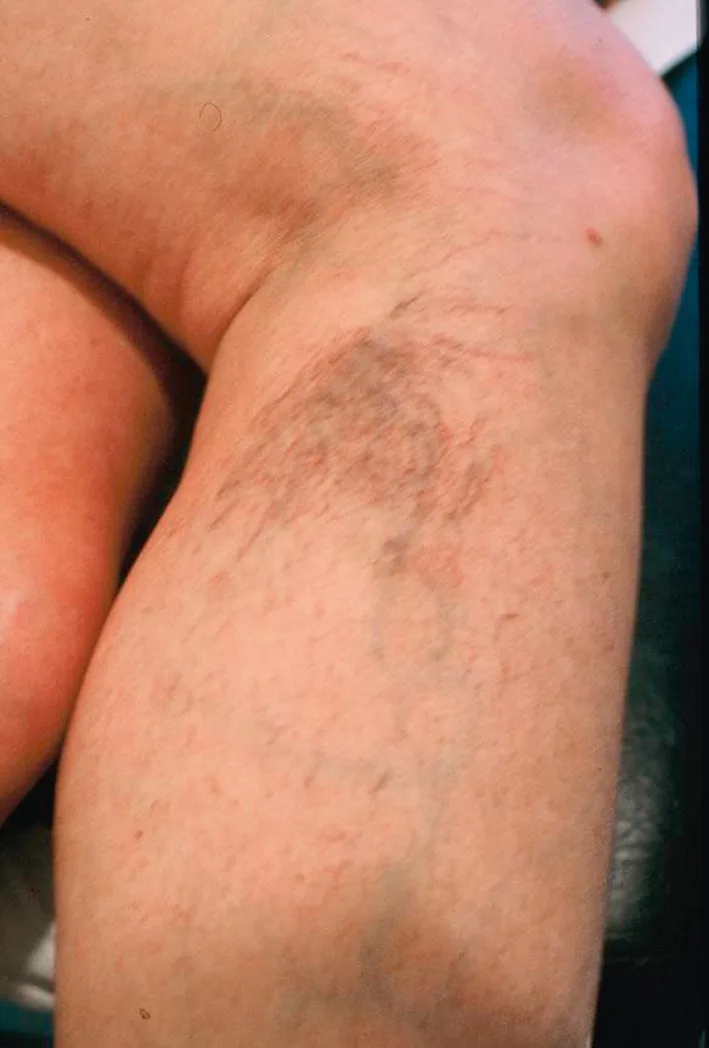
Fig. 3.2 S’ouvre dans une nouvelle fenêtre C1 : télangiectasies de la face latérale du mollet alimentées par une veinule sus-jacente.
Leur survenue secondaire – matting à un traumatisme, une sclérose ou un éveinage – est possible.
Certains patients rapportent une disparition des lourdeurs de jambes après sclérothérapie de leurs télangiectasies.
Seules certaines télangiectasies apparues pendant la grossesse peuvent régresser spontanément pendant le premier mois du post-partum ; les autres ont tendance à persister ou à augmenter spontanément.
Les télangiectasies des membres inférieurs proviennent souvent de l’IVS, les autres peuvent être congénitales ou acquises.
Les formes congénitales peuvent s’inscrire dans les maladies suivantes :
maladie de Rendu-Osler;
xeroderma pigmentosum;
ataxie télangiectasie;
angiome serpigineux;
poïkilodermie;
hypoplasie dermique en aires, etc.
Les formes acquises peuvent être associées à :
prise de poids importante et rapide ;
grossesse ;
cirrhose et cancer hépatique ;
glomérulonéphrite chronique ;
endocardite ;
maladie de Vaquez ;
lupus, sclérodermie, etc.
Les formes acquises cutanées sont les plus fréquentes :
peau sénile ;
atrophie après corticothérapie, radiodermite, exposition aux ultraviolets ;
traumatisme, éveinage, sclérose ;
capillarite chronique ;
télangiectasies essentielles.
Dans les télangiectasies essentielles, citons les télangiectasies essentielles progressives. Elles constituent une forme assez rare mais que chaque médecin vasculaire rencontre au moins une fois par an, surtout dans sa forme de début ou localisée dite « syndrome des chaussettes rouges » (fig. 3.3) [23].
Ce syndrome survient chez la femme après 40 ans, se développe au niveau du dos du pied pour s’étendre progressivement en direction crâniale. Il peut atteindre toute partie du derme, les muqueuses voire les conjonctives.
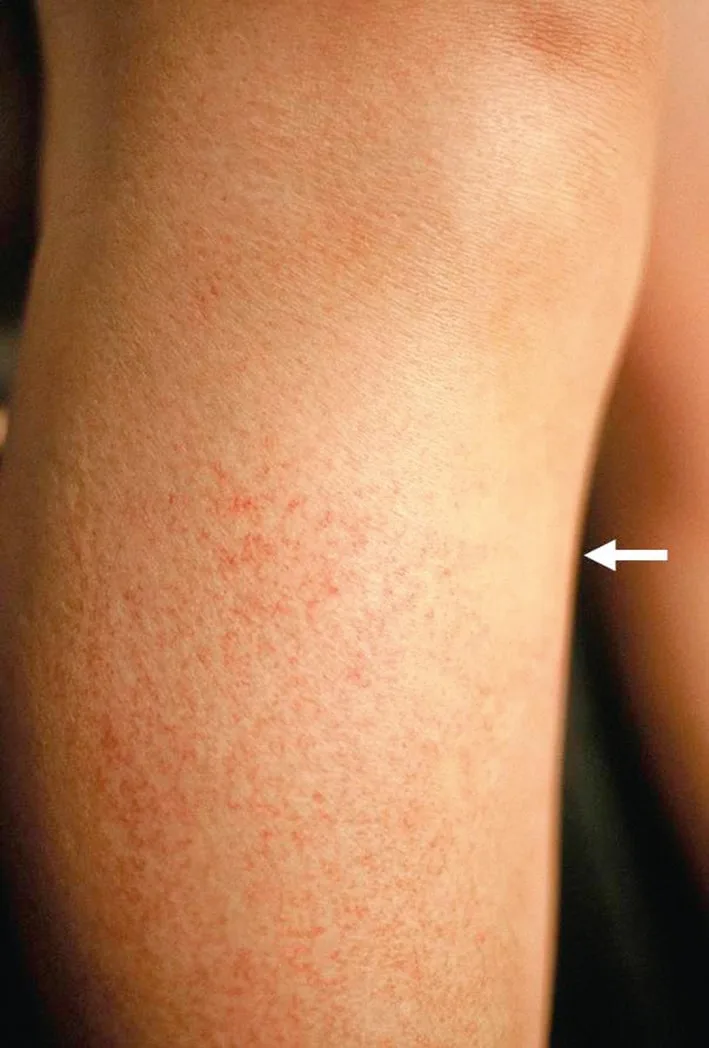
Fig. 3.3 S’ouvre dans une nouvelle fenêtre Syndrome des chaussettes rouges : limite horizontale des télangiectasies.
Typiquement, ce syndrome est bilatéral et comporte : une sensation d’échauffement, de bouillonnement des jambes et des pieds, sensation augmentée par la chaleur ; des télangiectasies très fines, très superficielles, en réseau réticulé et homogène, couvrant l’ensemble des téguments du dos des pieds, des chevilles et des jambes. La limite est parfois horizontale à quelques centimètres sous le genou donnant une impression visuelle de chaussettes rouges. Le reste de l’examen est normal, sans varices ; il n’existe pas d’anomalie biologique ; des formes unilatérales et des formes frustes, limitées à la région sus-malléolaire existent.
C1 : veines réticulaires
Veines ou varices réticulaires
Elles ont un diamètre compris entre 1 et 3 mm. Elles sont la transition entre les télangiectasies et les varices. Elles sont avant tout inesthétiques.
Certaines sont des veinules pathologiques comme les perles variqueuses et la couronne phlébectasique.
Si ces dernières ne font pas partie des items de la classification CEAP, elles sont presque toujours associées à des varices importantes.
Perles variqueuses
Le patient âgé est inquiet à juste titre devant des petites dilations ampullaires saillantes, bleu foncé, de 1 à 2 mm recouverte d’une peau amincie, siégeant sur le pied ou en partie basse de jambe. Ces perles sont en rapport avec des varices sus-jacentes à rechercher systématiquement. Elles sont la cause fréquente de thrombose in situ et d’hémorragie importante au moindre traumatisme. Le traitement des perles elles-mêmes et des varices attenantes est impératif du fait de leurs complications potentielles.
Couronne phlébectasique
La corona phlebectatica paraplantaris (fig. 3.4) consiste en l’association de dilatations vasculaires avec trois types de vaisseaux :
des télangiectasies intradermiques rouges ou bleues à disposition radiaire, centrées par la malléole médiale ;
des veinules sous-cutanées responsables des « dilatations cupuliformes » qui déforment la surface cutanée ;
des capillaires érythrocyaniques, sous la forme de « taches de stase », qui s’effacent à la vitropression.
La corona siège au niveau du cou-de-pied, prédomine le plus souvent dans la région sous-malléolaire médiale ; elle peut aussi s’étendre de manière circonférentielle autour du cou-de-pied.
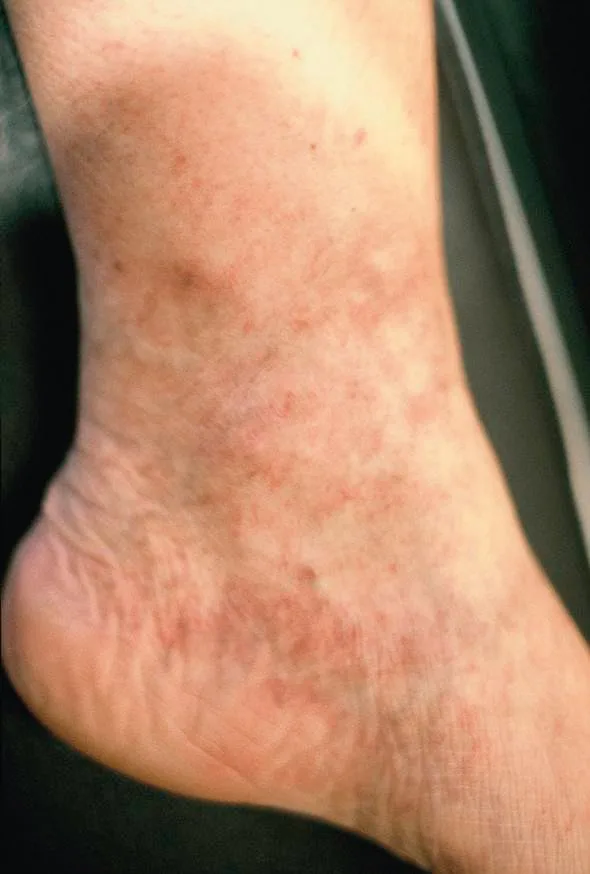
Fig. 3.4 S’ouvre dans une nouvelle fenêtre Corona phlebectatica et perforante sus-jacente.
Elle est à différencier de certains mattings secondaires à un choc, un hématome, une thrombose veineuse superficielle par l’absence de veinules en relief ; de certains bouquets de télangiectasies centrés par une perforante. Le caractère isolé permet donc cette différenciation.
Les sujets variqueux présentant une corona phlebectatica ont un risque de trouble trophique 6 fois plus élevé à 11 ans que ceux dont les varices ne s’accompagnent pas de ce signe. L’examen clinique et échographique recherche des varices sus-jacentes et notamment des perforantes jambières basses excentrées qui lui sont souvent associées [24–26].
C2 : varices
Cliniquement, on distingue les varices tronculaires ou interfasciales, d’inspection et de palpation difficiles, des varices des branches accessoires ou sus-fasciales, plus superficielles, souvent bien visibles et palpables.
Quatre veines ont un trajet interfascial : la grande veine saphène (GVS), la petite veine saphène (PVS) dans sa moitié supérieure, la partie haute de la saphène accessoire antérieure de cuisse et la partie basse de la grande anastomose intersaphénienne de Giacomini. Le seul examen clinique, même chez le sujet mince, ne permet pas toujours le diagnostic de varice tronculaire [27].
À l’inverse, les branches accessoires variqueuses sont saillantes en orthostatisme, bleutées sous la peau, avec un aspect contourné. Ces branches dépendent d’un reflux tronculaire, d’une perforante ou d’une tributaire.
La varicose des anastomoses intersaphéniennes permet qu’un reflux de tronc saphène se répercute d’un territoire saphénien à l’autre. Il s’agit alors d’un vol de territoire, source de difficultés pour retrouver la ou les origines d’un reflux.
À la fin de cet examen clinique, une cartographie veineuse [28] est réalisée dans le dossier du patient. Cette cartographie (fig. 3.5) sera confrontée aux résultats de l’examen écho-Doppler, modifiée et complétée par les mesures des diamètres veineux.
Devant des varices importantes, il convient de rechercher les facteurs de risque [29] pour l’apparition d’un ulcère veineux qui sont :
obésité ;
dorsiflexion limitée de la cheville ;
tabac (à partir de dix cigarettes/jour) ;
épisode de thrombose veineuse profonde (TVP) ;
corona phlebectatica ;
modification cutanée de la jambe (dermite ocre, eczéma, hypodermite scléreuse, atrophie blanche).
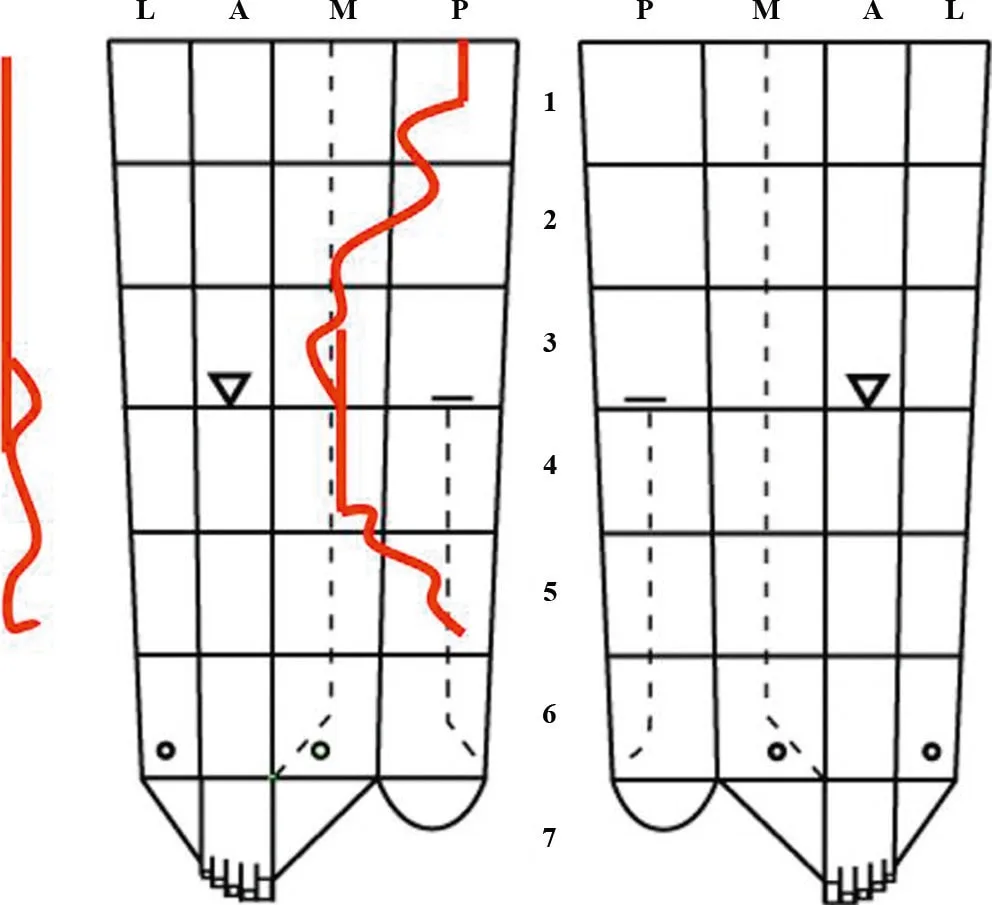
Fig. 3.5 S’ouvre dans une nouvelle fenêtre Cartographie veineuse. À droite : varicose du tronc GVS à la cuisse et d’une branche sus-fasciale au mollet. À gauche : varicose de la veine intersaphénienne de Giacomini alimentée par la GVS proximale ; varicose tronculaire de la PVS qui donne une branche superficielle à mi-mollet en direction de la malléole médiale. Index variqueux : 6 à droite et 8 à gauche.
Diagnostic différentiel des varices
Hernies piézogéniques de jambe
Isolées ou bilatérales et souvent symétriques, ces petites tuméfactions bien circonscrites des faces antérieures et latérales de jambe sont visibles chez le sujet debout. Leur caractéristique est de se modifier au cours des mouvements musculaires. Elles disparaissent à la dorsiflexion du pied, en position couchée ou à la compression manuelle. Il s’agit d’une saillie du tissu adipeux au travers d’une déhiscence fasciale.
Tumeurs bénignes de l’hypoderme
Certaines tumeurs sous-jacentes à une veine peuvent cliniquement avoir un aspect trompeur. L’examen écho-Doppler permet de conclure.
Veines anormalement visibles
La peau claire et fine permet de voir anormalement certaines veines. L’aspect ni tortueux, ni dilaté et l’absence de reflux au Doppler permettent de les différencier des varices. De même, les sujets maigres, anorexiques ou sous trithérapie qui présentent un panicule adipeux réduit ont des veines normales en relief.
Veines du sportif
Ici, la dilatation des veines est en rapport avec une augmentation du débit sanguin et une hypertrophie de la musculeuse pariétale de la veine. Ainsi chez les grands sportifs au panicule adipeux réduit, les veines superficielles apparaissent en relief.
À l’arrêt de la pratique sportive, la fonte musculaire de la paroi peut entraîner leur transformation en varices.
Fistule artérioveineuse
Les fortes augmentations de débit et de pression sanguine peuvent entraîner un développement anormal du réseau superficiel.
Topographies particulières des varices
Varices du pied
Le pied est le point le plus bas de la circulation veineuse. Il n’est pas le siège premier de varices.
Les varices du pied ne sont donc jamais isolées, elles sont toujours en rapport avec des reflux sus-jacents : reflux saphéniens, reflux de perforantes jambières.
La contribution au retour veineux de la semelle veineuse plantaire sous-dermique, constituée de vaisseaux minuscules, est physiologiquement insignifiante.
Les troncs veineux plantaires, profonds, compris entre le plan osseux et le fascia, constituent un réservoir sanguin qui, comprimé par la main d’un explorateur, donne un flux sus-jacent bien détecté au Doppler.
Cliniquement, les varices du pied intéressent les veines du dos du pied, réseau à mailles larges contenu en périphérie par les deux veines marginales, et les perforantes plantaires. L’inspection du sujet debout sur l’escabeau de phlébologie permet un diagnostic immédiat à la vue de ces veines volumineuses.
La palpation élimine toute induration de thrombose superficielle.
Un examen complet (clinique et écho-Doppler) du ou des membres inférieurs s’impose à la recherche du ou des reflux sus-jacents.
Souvent asymptomatiques, les varices du pied peuvent être le siège de douleurs parfois lancinantes, de démangeaisons, de difficultés au chaussage.
Ces varices sont souvent accompagnées de télangiectasies rouges ou bleutées, plus rarement de bulles variqueuses (perles noires).
On les distingue de :
la corona phlebectatica ;
l’angiome veineux congénital du dos du pied : son caractère isolé et présent dès l’enfance permet sa différenciation. On vérifie son caractère purement veineux à l’auscultation, à l’écho-Doppler couleur et au Doppler continu. On contrôle aussi l’absence de kyste synovial. En cas de gêne ou d’augmentation de taille de l’angiome, une phlébectomie ambulatoire peut être programmée par un opérateur de grande expérience.
Varices périnéales
Elles doivent être recherchées systématiquement lors de l’examen clinique en position debout, imposant une inspection minutieuse au niveau de l’entrejambe et parfois en tendant la peau médiale de la cuisse.
Très superficielles, leur diagnostic est facile.
Elles peuvent être associées à des varices pelviennes.
Elles sont souvent secondaires à une grossesse [30] ou à une crossectomie.
Elles peuvent être à l’origine d’un reflux tronculaire de la GVS, alors que la jonction saphénofémorale est continente. Ce vol de territoire peut être la cause d’erreurs de cartographie veineuse et de stratégie thérapeutique.
À la face postérieure de la cuisse, ces varices peuvent s’étendre jusqu’à la marge anale.
Varices vulvaires
Classiquement, les varices vulvaires apparaissent au 5e mois de la deuxième grossesse. Elles sont présentes chez 10 % des femmes enceintes. Par pudeur, les femmes en parlent peu et elles ne sont pas suffisamment recherchées en position debout à l’examen médical du 6e mois de grossesse et du 1er mois après la délivrance. Elles sont le plus souvent asymptomatiques. Douleurs, prurit, dyspareunies, gêne à la marche sont possibles pendant la grossesse. Thrombose et hémorragie restent rares.
Varices abdominales
Rarement isolées, elles doivent faire rechercher une thrombose ou une atrésie iliaque ou cave.
Varices de l’enfant et du sujet âgé
Hyperplasie des parois veineuses et turgescence veineuse sont détectables chez 10 % des enfants de 10 ans, et plus de 2 % de ces enfants présentent déjà des reflux de la GVS. Ce pourcentage de reflux augmente avec l’âge pour être de 20 % à 30 ans.
Classiquement, les enfants « variqueux » semblent préférer les positions allongées pour lire, travailler ou regarder la télévision.
Les complications des varices, fréquentes chez le sujet âgé, sont une grande cause de dégradation de leur qualité de vie et de la perte de leur autonomie. Cette potentialité impose un suivi clinique attentif et une éradication des varices pathogènes.
Récidive variqueuse après chirurgie
La récidive est la présence de veines variqueuses au niveau d’un membre inférieur précédemment opéré des varices, ayant bénéficié ou non d’un traitement complémentaire.
Cela inclut les varices résiduelles et les varices nouvellement apparues liées au geste chirurgical ou à l’évolutivité de la maladie.
La classification REVAS (recurent varices after surgery) publiée en 2000 est issue d’une réunion de consensus et nous aide dans notre démarche clinique. Elle présente six items :
topographie des sites de récidive : aine, cuisse, fosse poplitée, jambe ;
source de la récidive : absente, pelvienne ou abdominale, jonction saphénofémorale, perforantes de cuisse, jonction saphénopoplitée, perforantes poplitées, veines gastrocnémiennes, perforantes de jambe ;
reflux : probable (R +), incertain (R), peu probable (R −) ;
nature des sources du reflux : site opéré, site non opéré ;
contribution : existe-t-il un tronc saphène incompétent : GVS sus-gonale (fig. 3.6), GVS sous-gonale, PVS, aucune saphène ?
facteurs prédisposants :
général : hérédité, grossesse, traitement hormonal,
spécifique : insuffisance veineuse profonde, syndrome post-thrombotique, compression de la veine iliaque, angiodysplasie, dysfonction des pompes musculaires.
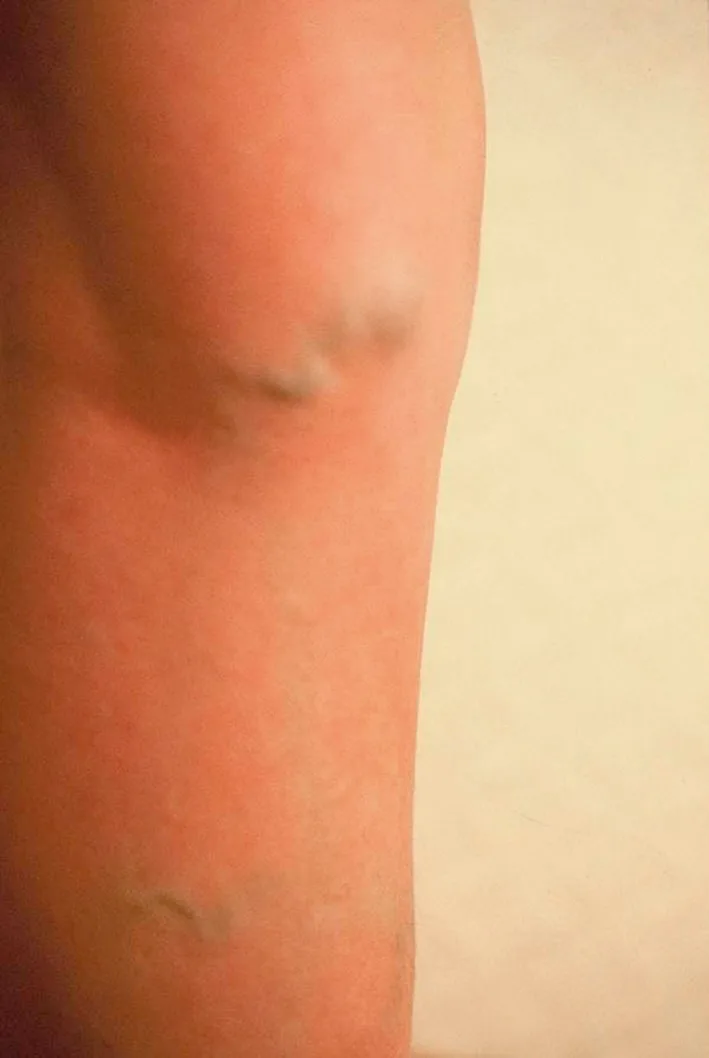
Fig. 3.6 S’ouvre dans une nouvelle fenêtre C2 : varice sus-gonale en face médiale.
Pour répondre à ces six items, l’examen est clinique et écho-Doppler.
En consultation devant un patient présentant une récidive [31], nous nous posons d’emblée trois questions :
s’agit-il de varices essentielles ? Devant un échappement au traitement, avons-nous fait au départ le bon diagnostic, s’agit-il réellement de varices essentielles ? Depuis l’intervention existe-il des facteurs prédisposants locaux comme une TVP ou une fistule artérioveineuse (6e item de la classification REVAS) ? Cette recherche impose un écho-Doppler ;
quel est le degré de confiance du patient dans les traitements (éveinage, sclérose, etc.) ?Quel est l’état d’esprit du patient suite à cet échec thérapeutique ? Le plus simple est de lui demander si l’intervention s’est bien passée pour aborder le sujet… En fin de consultation, si le traitement indiqué est à l’opposé des désirs du patient, nous aborderons ce problème de confiance ;
quelle est la nouvelle cartographie veineuse ? Il convient bien sûr d’établir cette nouvelle cartographie pour ce nouvel état des lieux et d’essayer de comprendre le mécanisme et l’importance de la récidive pour proposer au mieux une stratégie thérapeutique.
Cette cartographie permet de répondre aux cinq premiers items de la classification REVAS. Même si l’examen clinique se fait toujours des orteils à la ceinture, nous allons suivre ici la topographie REVAS :
aine : noter la localisation exacte de la cicatrice de crossectomie, des varices sus-fasciales ; rechercher par la palpation–percussion une crosse en place. Rechercher aussi à l’entrejambe des varices pelviennes résiduelles ou secondaires à la crossectomie. L’absence d’un intervalle libre après l’intervention est en faveur d’une varice résiduelle ;
cuisse : l’examen recherche des perforantes, des varices sus-fasciales, un développement anormal de la saphène accessoire antérieure de cuisse ou de la saphène accessoire postérieure de cuisse ;
fosse poplitée : le cavernome est d’un diagnostic facile. Il est constitué d’un amas d’ectasies veineuses multiples, de dimensions variables, de parois fines et fragiles. Ce cavernome au voisinage d’une cicatrice est parfaitement visible et palpable ; il est plus rare au niveau de l’aine. Nous recherchons aussi par la palpation–percussion une crosse en place, des perforantes de la fosse poplitée… ;
jambe : on note la ou les cicatrices (stripping long ou court) et leurs varices attenantes. Parfois une varice semble sortir d’une contre-incision. Notre attention se porte sur les perforantes excentrées du tiers inférieur de jambe en face médiale et à mi-mollet en face postérieure (fig. 3.7).
Fig. 3.7 C1 : télangiectasies de la face médiale de la cuisse alimentées par une perforante.
Au terme de cet examen clinique, la cartographie commence à se mettre en place, elle sera complétée par l’examen écho-Doppler.
L’analyse de cette cartographie permet fréquemment de retrouver, dans un même territoire opéré, des varices qui résultent de plusieurs mécanismes de formation : varices résiduelles, collatéralité, néogenèse et évolutivité de la maladie.
C3 : œdème
Devant ce motif fréquent de consultation, il convient de poser au patient la question suivante : « Actuellement, vos jambes sont-elles gonflées ? »
Cela permet de quantifier ce signe clinique cutané objectif et de le différencier d’une sensation de gonflement.
La mesure des diamètres en centimètre quantifie ce signe objectif. Les mesures se font :
au-dessus des malléoles : périmètre minimal ;
aux mollets : périmètre maximal ;
aux cuisses : 15 cm au-dessus du bord supérieur de la rotule.
On en profite pour mesurer les hauteurs pour la prescription d’un traitement compressif :
distance sol–pli poplité ;
distance sol–entrejambe.
Classiquement, on retrouve, en faveur d’un œdème lié à une insuffisance veineuse chronique superficielle, un œdème périphérique :
souvent asymétrique, respectant les orteils ;
à prédominance vespérale ;
disparaissant par la position déclive ou le traitement compressif, amélioré par les médicaments veino-actifs.
L’examen clinique recherche une varice importante en rapport avec cet œdème.
L’étiologie des œdèmes uni- ou bilatéraux n’est pas univoque.
Face à un patient porteur d’un lipœdème et ayant un discours de « rétention d’eau » et de « problèmes circulatoires », l’échographie a un intérêt pédagogique pour permettre à ce dernier de visualiser les plages de graisse, blanches à l’écran.
L’œdème du voyageur dû à une immobilité en position assise et à un climat chaud est parfois associé à une sciatalgie. Cette association douleur–œdème, trompeuse, impose parfois d’éliminer une thrombose.
C4 : troubles trophiques
Il s’agit d’altérations de la peau (épiderme, derme, hypoderme) et des tissus cellulaires sous-cutanés.
On distingue les :
troubles réversibles(C4a) : eczéma, pigmentation ;
troubles irréversibles(C4b) : hypodermite scléreuse (lipodermatosclérose), atrophie blanche.
Les complications cutanées de l’IVS sont généralement peu spécifiques. Ainsi, devant un motif cutané de consultation, si l’examen ne retrouve pas une varicose importante sus-jacente, il convient de rechercher activement une autre étiologie.
Eczéma variqueux
Typiquement, il s’agit, souvent à la face antéromédiale de la jambe, d’un eczéma localisé en regard d’une varice sus-fasciale bien visible. L’eczéma est une dermatose prurigineuse, érythématovésiculeuse, plus ou moins suintante, en nappes ou en placards. Il résiste aux crèmes corticoïdes ou récidive, mais guérit rapidement après éradication de la varicose et/ou le port d’un traitement compressif.
Par ailleurs, l’eczéma est une dermite inflammatoire fréquente, favorisée dans l’IVS par la stase qui peut prendre de multiples aspects peu spécifiques : citons une forme péri-ulcéreuse liée aux topiques ou aux bactéries, un eczéma de l’avant-pied lié à une mycose des ongles ou des orteils, un eczéma sus-malléolaire médial qui s’étend en nappes sur l’ensemble de la jambe, un eczéma jambier de contact qui devient disséminé au haut du corps… Ce polymorphisme semble peu spécifique de l’IVS.
Dermite ocre
Elle est formée de petites taches brunes ou de grandes nappes coalescentes, émiettées à leur périphérie, rouges pourpres, puis brunes. Elle siège à la face antéro-externe de la jambe, en partie basse ou parfois en regard d’un trajet variqueux. Cette dermite est précédée d’un purpura pétéchial ne s’effaçant pas à la vitropression due à une extravasation de globules rouges.
Cette angiodermite purpurique et pigmentée de Fabre et Chaix est due à une double pigmentation d’hémosidérine et de mélanine. Le stade de purpura et de dermite ocre coexiste donc souvent.
En l’absence de varicose importante, on évoquera les pigmentations post-lésionnelles, les colorations iatrogènes (après sclérothérapie par exemple) et les purpuras aux nombreuses étiologies.
Hypodermite scléreuse
Cette dermite touche avant tout le sujet féminin, de la cinquantaine, en surpoids et présentant une pathologie veineuse [32].
Classiquement irréversible, l’hypodermite scléreuse débute à la face médiale de jambe, en sus-malléolaire par un placard dur, rose, infiltré adhérant au plan profond. Ce placard s’étend naturellement vers le haut et de manière circonférentielle pour créer au maximum une guêtre scléreuse dite en « bouteille de champagne ». À ce stade la peau est lisse, dure, fine, brillante, parfois pigmentée, bigarrée et impossible à plisser.
Parfois des varices « canyon » sont visibles en creux et palpables sous la surface de la guêtre.
Cette inflammation chronique peut être associée à une rétraction ou un raccourcissement du tendon d’Achille, ce qui diminue la dorsiflexion de la cheville et aggrave l’IVS.
Au stade aigu, cette hypodermite est donc une urgence médicale afin de préserver la fonctionnalité du membre et l’intégrité de la peau.
L’absence d’adénopathies, d’érythème franc et de fièvre permet de différencier l’hypodermite de l’érysipèle ou d’une cellulite aiguë. Néanmoins, la décompensation aiguë de l’hypodermite scléreuse peut être difficile à différencier d’une infection.
De même, la différenciation entre hypodermite et thrombose veineuse saphénienne ou tibiale basse au stade de début d’un placard inflammatoire sus-malléolaire peut être difficile, l’écho-Doppler aidant au diagnostic différentiel.
Atrophie blanche
Souvent périmalléolaire, l’atrophie blanche commence par des macules purpuriques qui évoluent vers des cicatrices blanches, lisses et déprimées, entourées par des télangiectasies et une couronne pigmentée. Plus fréquente chez la femme, elle peut se compliquer d’ulcérations (voire d’un ulcère).
En l’absence d’une hyperpression veineuse (insuffisance veineuse superficielle ou post-thrombotique), il convient de rechercher une connectivite, une péri-artérite noueuse, tout en sachant que la forme idiopathique chez la femme jeune est rare.
Ces atteintes dermiques sclérorétractiles sont à différencier des zones cicatricielles d’un ancien ulcère.
C5 : ulcère cicatrisé
Sus-malléolaire en face médiale de jambe, la cicatrice d’un ulcère pose peu de problème diagnostique. Le tissu cicatriciel blanchâtre, à ne pas confondre avec une atrophie blanche, est souvent entouré d’une zone pigmentée.
Parfois il faut convaincre le patient de laisser la peau à l’air pour permettre la désquamation physiologique de la peau.
L’examen clinique va à la recherche des facteurs de récidive d’un ulcère à prédominance veineuse, à savoir : des varices en place, résiduelles ou récidivées ; des veinules péri-ulcéreuses ; une modification cutanée de la jambe ; un surpoids ; un tabagisme ; une inactivité physique et une limitation de la dorsiflexion du pied. Ces facteurs doivent impérativement être corrigés dans la mesure du possible, les varices et les veinules doivent être complètement éradiquées. Le port d’une compressothérapie à vie est discuté.
C6 : ulcère de jambe
L’ulcère variqueux ouvert ou actif est le stade clinique le plus évolué de la maladie veineuse chronique [33, 34]. Un ulcère variqueux de la jambe, actif ou guéri, est présent chez 1 % de la population des pays développés.
Les ulcères variqueux sont généralement douloureux et affectent la qualité de vie.
La dépression, l’isolement social, la perte de la notion d’hygiène corporelle et vestimentaire peuvent aboutir à une véritable « clochardisation » du patient porteur d’un ulcère variqueux ouvert.
Il s’agit donc d’une véritable urgence médico-sociale.
Scores cliniques
Peu de scores sont spécifiques de l’IVS.
Douleur
Le score clinique pour caractériser une douleur veineuse a été vu plus haut (voir C0, S : douleurs des membres inférieurs).
Les mesures d’intensité des douleurs de l’IVS ne sont pas spécifiques. Pour ces mesures, les échelles analogiques sont couramment utilisées.
On en rapproche les questionnaires de qualité de vie [35, 36] comme ceux de Launois ou de Franks [37, 38].
Varices
Les items de la classification CEAP ne sont pas mesurables. Cette dernière n’a pas été conçue pour permettre une évaluation chiffrée de la maladie. Pour cela, il faut lui adjoindre des scores de sévérité.
Le C2 de la classification clinique de la CEAP indique simplement la présence de varices, mais ne donne aucune indication sur l’importance de ces varices (nombre, diamètres) ; il n’existe actuellement aucun score pour quantifier celles-ci. Ce score manque cruellement pour l’évaluation des traitements d’éradication des varices (éveinage, sclérose, etc.) Pour cette quantification, il a été proposé de mesurer le plus grand diamètre variqueux [39, 40] ou encore, après avoir réalisé une cartographie « peau à plat » sur quadrillage, de compter pour un point chacun des 28 quadrilatères présentant au moins une varice pour en déduire un index variqueux pour chaque membre inférieur [41].
Insuffisance veineuse chronique
Un score de sévérité a été ajouté à la classification CEAP, il concerne l’IVC. Ce score est basé sur trois éléments :
anatomique : on compte pour un point le nombre de segments affectés des 18 segments anatomiques de la classification CEAP. Ce score mélange donc les veines abdominales, les veines superficielles, musculaires et profondes des membres inférieurs sans oublier les veines perforantes ;
clinique : on cote de 0 à 3 chacun des dix signes ou symptômes suivants : douleur, varices, œdème, pigmentation cutanée, inflammation, induration, nombre d’ulcères actifs, durée de l’ulcère actif, taille de l’ulcère actif, traitement compressif ;
invalidité : elle est cotée de 0 à 3, de asymptomatique à impossibilité de travailler même avec une compression.
Ce score de sévérité s’il prend bien en compte l’ensemble de la maladie veineuse, est peu spécifique pour évaluer les traitements d’éradication des varices et leurs récidives.
Références [1] Uhl JF, Cornu-Thénard A, Antignani PL, Lefloch E. Importance du motif de consultation en phlébologie. Phlébologie 2006 ; 59(1) : 47–51. [2] Bergman JJ, Schmid-Schönbein W, Smith PD, et al. Chronic venous disease. N Engl J Med 2006 ; 355(5) : 488–98. [3] Cornu-Thenard A, Boivin P, Baud JM, et al. Importance of the familial factor in varicose disease. J Dermatol Surg Oncol 1994 ; 20 : 318–20. [4] Brand FN, Dannenberg AL, Abbott RD, Kannel WB. The epidemiology of varicose veins : the Framingham Study. Am J Prev Med 1988 ; 4 : 96–101. [5] Evans CJ, Fowkes FGR, Ruckley CV, Lee AJ. Prevalence of varicose veins and chronic venous insufficiency in men and women in the general population : Edinburgh Vein Study. J Epidemiol Community Health 1999 ; 53 : 149–53. [6] Kurz X, Kahn SR, Abenhaim L, et al. Chronic venous disorders of the leg : epidemiology, outcomes, diagnosis and management : summary of an evidence-based report of the VEINES task force. Int Angiol 1999 ; 18 : 83–102.[7] Labropoulos N. Hemodynamic changes according to the CEAP classification. Phlebolymphology 2003 ; 40 : 130–6. [8] Allaert FA. Pharmaco-épidémiologie de la prise en charge de l’insuffisance veineuse chronique en médecine générale. Angéologie 2006 ; 58(1). [9] Thierry L. La douleur veineuse. Phlébologie 1988 ; 41(3) : 673–8. [10] Remacle J, et al. Relation entre la stase veineuse et l’apparition de la douleur. Phlébologie 1991 ; 45(1) : 33–9.[11] Carpentier PH, Cornu-Thénard A, Uhl JF, et al. Appraisal of the information content of the C classes of CEAP clinical classification of chronic venous disorders : a multicenter evaluation of 872 patients. J Vasc Surg 2003 ; 37 : 827–33. [12] Juhan C, Barthélemy P, Alimi Y. Diversité des étiologies des jambes lourdes sans varice. JAMA avril 1995 ; 2–6 hors séries. [13] Danziger N. Physiopathologie de la douleur au cours de la maladie veineuse. Le Concours Médical 2004 ; 26 : 1521–5. [14] Nemeth KA, Harrison MB, Graham ID, Burke S. Understanding venous leg ulcer pain : results of a longitudinal study. Ostomy Wound Manage 2004 ; 50 : 34–46. [15] Hauer G. Diagnosis and surgical management of varicosities. Herz 1989 ; 14(5) : 274–82. [16] Allegra A, Antignani PL, Bergman JJ, et al. The C of the CEAP : suggested definitions and refinements. An International Union of Phlebology conference of experts. J Vasc Surg 2003 ; 37 : 129–31. [17] Kistner RL, Eklof B, Masuda EM. Diagnosis of chronic venous disease of the lower extremities : the « CEAP » classification. Mayo Clin Proc 1996 ; 71 : 338–45. [18] Eklof B, Rutherford RB, Bergan JJ, et al. Revision of the CEAP classification for chronic venous disorders : consensus statement. J Vasc Surg 2004 ; 40 : 1248–52. [19] Cornu-Thénard A, Uhl JF, Carpentier PH. Do we need a better classification than CEAP ? Acta Chir Belg 2004 ; 104(3) : 276–82. [20] Antignani PL, Cornu-Thénard A, Allegra C, et al. European Working group on venous classification under the auspices of the International Union of Phlebology. Results of a questionnaire regarding improvement of ‘C’ in the CEAP classification. Eur J Vasc Endovasc Surg. 2004 ; 28(2) : 177–81. [21] Schultz-Ehrenburg U, Matthes U. Telangiectasis after varicose vein exeresis. Hautarzt 1992 ; 43(1) : 51. [22] Coleridge Smith PD. The microcirculation in venous hypertension. Vasc Med 1997 ; 2(3) : 203–13. [23] Van Cleef JF. Le syndrome des chaussettes rouges. Phlébologie 1994 ; 47(4) : 307–9. [24] Cohn JD, Korver KF. Selection of saphenous vein conduit in varicose vein disease. Ann Thorac Surg 2006 ; 81(4) : 1269–74. [25] Hagmüller GW, Denck H. Operation on varicose, especially in the malleolar region. Wien Klin Wochenschr 1976 ; 88(12) : 388–90. [26] Uhl JF, Cornu-Thénard A, Carpentier PH, et al. Clinical and hemodynamic significance of corona phlebectatica in chronic venous disorders. J Vasc Surg 2005 ; 42(6) : 1163–8. [27] Porter JM, Moneta GL. Reporting standard in venous disease : an update. J Vasc Surg 1995 ; 21 : 635–45.[28] Van Cleef JF, Auvert JF. Cartographie pré-thérapeutique informatisée. Phlébologie 1999 ; 52(1) : 78–80.[29] Robertson L, Lee AJ, Gallagher K, et al. Risk factors for chronic ulceration in patients with varicose veins : a case control study. J Vasc Surg 2009 ; 49(6) : 1490–8. [30] Dindelli M, Parazzini F, Basellini A, et al. Risk factors for varicose disease before and during pregnancy. Angiology 1993 ; 5 : 361–7. [31] Van Cleef JF. Aspects cliniques des récidives variqueuses après chirurgie. Phlébologie 1998 ; 51(4) : 397–400. [32] Bruce AJ, Bennett DD, Lohse CM, et al. Lipodermatosclerosis : review of cases evaluated at Mayo Clinic. J Am Acad Dermatol 2002 ; 46(2) : 187–92. [33] Moffatt CJ, Franks PJ, Doherty DC, et al. Prevalence of leg ulceration in a London population. QJM 2004 ; 97 : 431–7. [34] Ruckley CV. Socioeconomic impact of chronic venous insufficiency and leg ulcers. Angiology 1997 ; 48 : 67–9. [35] Kahn SR, M’lan CE, Lamping DL, et al. Relationship between clinical classification of chronic venous disease and patient-reported quality of life : results from an international cohort study. J Vasc Surg 2004 ; 39 : 823–8.[36] Kaplan RM, Criqui MH, Denenberg JO, et al. Quality of life in patients with chronic venous disease : San Diego Population Study. J Vasc Surg 2003 ; 37 : 1047–53. [37] Franks PJ, Wright DDI, Fletcher AE, et al. A questionnaire to assess risk factors, quality of life, and use of health resources in patients with venous disease. Eur J Surg 1992 ; 158 : 149–55. [38] Launois R, Reboul Marty J, Henry B. Construction et évaluation d’un indicateur spécifique de qualité de vie. Le cas de l’insuffisance veineuse chronique des membres inférieurs. J Econom Med 1994 ; 12 : 109–26. [39] Cornu-Thénard A, Boivin P, Garde C, Sentou Y. Évaluation des résultats des thérapeutiques curatives des varices par trois scores : clinique. Doppler et échographique. Phlébologie 1992 ; 45(4) : 389–99. [40] Cornu-Thénard A, Boivin P, Parpex P, et al. Essai d’une quantification clinique des varices pour l’épidémiologie, la thérapeutique et l’informatique. Phlébologie 1986 ; 39(3) : 661–76. [41] Taieb JC. Index variqueux ou quantification du C2 de la CEAP. Mémoire de capacité d’Angiologie. Faculté Paris-V ; 2009.
© 2015, Elsevier Masson SAS. Tous droits réservés
Vous venez de lire le Chapitre 3 Clinique et score de l’ouvrage La maladie veineuse chronique
Auteur de ce chapitre :
Jean-François Van Cleef médecin vasculai , institut Arthur Vernes, 43 rue de la Chaussée d’Antin, 75009 Paris.
Cet ouvrage est sous l’égide de Société Française de Médecine Vasculaire, Collège des enseignants de médecine vasculaire, Collège Français Pathologie Vasculaire
Coordinateurs de l’ouvrage
Jean-Louis Guilmot professeur de médecine vasculaire, 10 rue François Brocherioux, 37540 Saint-Cyr-sur-Loire.
Claudine Hamel-Desnos médecin vasculaire, hôpital privé Saint-Martin, 18 rue des Roquemonts, 14000 Caen.
Cet ouvrage est épuisé. Son contenu est intégré dans l'ouvrage de 2021
Traité de médecine vasculaire - Offre Premium S’ouvre dans une nouvelle fenêtre
Découvrez nos ouvrages en médecine vasculaire S’ouvre dans une nouvelle fenêtre